
Гліцерин
| Гліцерин | |
|---|---|
| |

| |

| |
| Систематична назва | пропан-1,2,3-тріол |
| Інші назви | Гліцерол |
| Ідентифікатори | |
| Номер CAS | 56-81-5 |
| PubChem | 753 |
| Номер EINECS | 200-289-5 |
| DrugBank | DB04077 |
| KEGG | D00028 і C00116 |
| ChEBI | 17522 |
| RTECS | MA8050000 |
| Код ATC | A06AX01 і A06AG04 |
| SMILES | C(C(CO)O)O |
| InChI | InChI=1S/C3H8O3/c4-1-3(6)2-5/h3-6H,1-2H2 |
| Номер Бельштейна | 635685 |
| Номер Гмеліна | 26279 |
| Властивості | |
| Молекулярна формула | C3H8O3 |
| Молярна маса | 92,09 г/моль |
| Зовнішній вигляд | безбарвна рідина гігроскопічна |
| Густина | 1,261 г/см3 |
| Тпл | 17,8 °C |
| Ткип | 290 °C |
| Кислотність (pKa) | ~14 |
| Небезпеки | |
| MSDS | JT Baker |
| NFPA 704 | |
| Температура спалаху | 160 °C (в закритій посудині) 176 °C (у відкритій посудині) |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
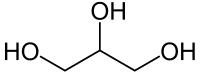
Гліцери́н (гліцеро́л) — триатомний спирт. Це означає, що в молекулі цього спирту три гідроксильні групи приєднані до трьох атомів вуглецю. Хімічна формула — C3H8O3, або C3H5(OH)3.
Зміст
Історія
Гліцерин відкрив у 1783 році шведський хімік Карл Вільгельм Шеєле, який показав, що фрагменти цієї сполуки складають основу всіх природних жирів, і назвав його «солодкою речовиною із жиру», позаяк продукт має солодкий смак. Шеєлє кип'ятив оливкову олію з окисом свинцю (свинцевий гліт). Визначити точний склад і будову цих фрагментів Вільгельм Шеєле не зміг — органічна хімія лише починала розвиватися.
У 1813 (1823) році французький хімік Мішель Ежен Шеврель встановив, що під дією води (каталізатори: кислота і луг) відбувається розщеплення жирів з утворенням гліцерину і вищих карбонових кислот. Він уперше дав назву «гліцерин» одному з продуктів, який утворюється в даному процесі («гліцерос» — солодкий). Французові Т. Петлузові в 1836 році вдалося встановити елементний склад цього тріолу.
Синтез гліцерину вперше провів у 1873 році французький хімік і мінеролог Ш. Фрідель.
Фізичні властивості
Чистий гліцерин являє собою прозору, безбарвну, дуже густу, в'язку, сиропоподібну, без запаху, важчу за воду і неотруйну солодкувату на смак рідину.
Гліцерин має здатність поглинати вологу з повітря та утримувати її. На повітрі може увібрати до 40% води від своєї маси. Таку властивість речовини називають гігроскопічністю. Через це гліцеринова крапля на руці дає враження легкого нагріву.
Питома вага хімічно чистого гліцерину при 15оС становить 1,26469.
Молекулярна маса 92,09 г/моль.
При звичайному атмосферному тиску гліцерин кипить при 290 °C і частково розкладається; під розрідженим тиском його можна перегнати, не розклавши. Змішується з водою в будь-якій пропорції. Як і при утворенні спирто-водних розчинів, при змішуванні гліцерину і води сумарний об'єм стає меншим, ніж об'єм вихідних компонентів.Температура спалаху гліцерину становить 150 °C, температура самозаймання — 362 °C. Як і винний спирт він горить не яскравим синім полум'ям. При нагріванні гліцерин швидко випаровується, а у звичайних умовах — гліцерин не леткий.
Гліцерин має здатність розчиняти різні мінеральні солі, через що чистий гліцерин добувається головним чином шляхом перегонки.
Від сильного і тривалого охолодження гліцерин кристалізується; температура плавлення кристалів — 20 °C. Гліцерин може залишатись рідким і при температурі нижче 0 ° — подібним чином себе поводять його водні розчини, наприклад, розчин, в якому на дві вагові частини гліцерину приходиться одна частина води, замерзає при температурі мінус 46,5 °. Гліцерин вповільнює утворення кристалів льоду.
Густина 1,261 г/см3 при 20 °C. Показник заломлення nD=1,4735 при 20 °C. Діелектрична проникність ε=42,5 при 25 °C. Дипольний момент молекули в газовому стані μ=2,56 Дб. В'язкість 9450 мПз.
Отримання
Синтетичним шляхом гліцерин отримують з пропену:
Взаємодією жиру із лугом можна отримати гліцерол і сіль вищої карбонової кислоти - реакція омилення жирів.
Похідні гліцерину завжди є в організмах вищих тварин і людини. Ці жири — складні ефіри гліцерину і органічних кислот (пальмітинової, стеаринової і олеїнової) — найенергоємніші речовини організму. Енергетична цінність гліцеридів у два з гаком рази більша, ніж у вуглеводів.
Гліцерин високого ступеня чистоти (не менше 98%) отримують шляхом алкоголізу рослинних жирів, із застосуванням вакуум-ректифікації. При остаточному тиску 400Па при температурі кипіння 130-140оС вдається уникнути полімеризації і термічного розкладання гліцерину з отриманням дистильованого продукту.
До розробки синтетичних методів гліцерин отримували лужним омиленням жирів. При цьому утворюються мила з водним розчином гліцерину. Мило відокремлюють шляхом висолювання за допомогою хлориду натрію, а гліцерин отримують шляхом повторного згущення і кристалізації осадженого хлориду натрію. Отриманий 80% гліцерин темного кольору очищується перегонкою і обробкою активованим вугіллям.
Існує ферментативний метод отримання гліцерину. Гліцерин присутній в натуральних винах, але у долях відсотка. Близько трьох відсотків цукру, який міститься у винограді, у кінцевому результаті перетворюються в гліцерин. В процесі дозрівання вина гліцерин частково перетворюється в інші органічні продукти.
Інший метод оснований на гідролітичному розщепленні вуглеводів (крохмалю, деревного борошна і цукру, особливо тростинного), призводить до утворення суміші гліцерину з іншими гліколями.
Також гліцерин утворюється при виробництві біодизеля.
Хімічні властивості
З водою гліцерин змішується в усіх пропорціях, причому об'єм такого розчину буде трохи менший від суми первинних об'ємів води й гліцерину. В усіх пропорціях змішується з етанолом. Не розчиняється в жирах, олії, бензині, хлороформі.
Наявність гідроксильних груп зумовлює подібність гліцерину до одноатомних спиртів, він вступає в ті самі реакції, але за участю трьох гідроксильних груп.
Реакції повного окиснення (горіння) відбувається, як і в інших органічних речовин, з утворенням вуглекислого газу і води.
Гліцерин вступає в реакцію заміщення з металічним натрієм, яка супроводжується виділенням водню.
Реакція з гідроксидами металів. На відміну від одноатомних спиртів, багатоатомні взаємодіють із гідроксидами лужних і металічних елементів.
Реакції
- Горіння:

- Взаємодія з металічним натрієм:

- З нерозчинними основами:
Застосування в промисловості
У промисловості його отримують головним чином при гідролітичному розщепленні жирів. Гліцерин випускають трьох видів — сирий, дистильований та технічно чистий. В косметиці дозволено застосування двох останніх. Гліцерин гігроскопічний. Завдяки властивості поглинати з повітря до 40—50 % води по відношенню до його початкової маси, він отримав широке розповсюдження в косметиці, як речовина, що швидко відбирає воду з тваринної та рослинної тканини. Він застосовується майже у всіх косметичних препаратах як пом'якшуючий засіб та є одним з основних видів сировини для виготовлення зубних паст. Він не засихає, не гіркне, замерзає при дуже низьких температурах і тому застосовується як речовина, що перешкоджає висиханню та замерзанню косметичних виробів.
Гліцерин використовується в парфумерії та фармації як пом'якшувальний засіб або основа мазей, добавка до масла, у харчовій промисловості — як добавка до напоїв (особливо, алкогольних). Наприклад, добавку гліцерину передбачає класична технологія приготування хорошого портвейну. Спиртовий розчин тринітрогліцерину має судинорозширювальну дію й у вигляді ліків використовується при серцевих захворюваннях. Похідним гліцерину є гліцерофосфат (гліцерофосфат кальцію і гліцерофосфат натрію), який використовують в медичній практиці. Із гліцерину синтетичним шляхом отримують незамінну амінокислоту метіонін, котру в медичній практиці застосовують при захворюваннях печінки і атеросклерозі.
Гліцерин, його олігомери і полімери запропоновані як засоби, які зберігають свіжість харчових продуктів.
У шкіряному виробництві та текстильній промисловості — для обробки пряжі і шкіри з метою їх пом'якшення та надання еластичності. Гліцерин застосовується в тютюновій промисловості, при виробництві поліуретанів, гуми, фанери, барвників, чорнил і паст, зубної пасти, емульгаторів, фотографічних і інших матеріалів. Гліфталеві смоли — продукти реакції гліцерину з фталевою кислотою, — будучи розчинені в спирті, перетворюються в хороший, хоча і дещо крихкий, електроізоляційний лак. Гліцерин необхідний для виробництва епоксидних смол — з гліцерину отримують епіхлоргідрин — незамінну речовину для синтезу епоксидної смоли.
З гліцерину добувають вибухову речовину тринітрогліцерин, що використовується для виготовлення динаміту. Роль гліцерину при виробництві пороху другорядна, але гліцерин є незамінною сировиною для отримання нітрогліцерину, а значить і балістичного пороху і динаміту.
Гліцерин як кормова добавка підвищує надої молока.
Гліцерин разом з пропіленгліколем формують основу рідини для паління в електронних сигаретах.
Література
- Фармацевтична хімія : [арх. 11 березня 2021] : підручник / ред. П. О. Безуглий. — Вінниця : Нова Книга, 2008. — 560 с. — ISBN 978-966-382-113-9. (С.78,79,82,95,100,102,117,123,133,138,139-141, 173-175,177,178,204,211,217,219,221,410,482)



