Камфора
| Камфора | |
|---|---|
|
Структурна формула камфори
|
Просторова модель молекули камфори ((1R,4R)-1-метил, гептан)
|
| Назва за IUPAC | 1,7,7-триметилбіцикло[2.2.1]гептан-2-он |
| Систематична назва | 1,7,7-триметилбіцикло[2.2.1]гептан-2-он |
| Інші назви | 2-борнанон; борнан-2-он; 2-камфанон; Формоза |
| Ідентифікатори | |
| Номер CAS | 76-22-2 |
| PubChem | 2537 |
| Номер EINECS | 200-945-0 |
| DrugBank | DB01744 |
| KEGG | D00098 |
| Назва MeSH | Camphor |
| ChEBI | 36773 |
| RTECS | EX1225000 |
| Код ATC | C01EB02 |
| SMILES | CC1(C)C2CCC1(C)C(=O)C2 |
| InChI | 1/C10H16O/c1-9(2)7-4-5-10(9,3)8(11)6-7/h7H,4-6H2,1-3H3 |
| Номер Бельштейна | 1907611 |
| Номер Гмеліна | 83275 |
| 3DMet | B04729 |
| Властивості | |
| Молекулярна формула | C10H16O |
| Молярна маса | 152,23 г/моль |
| Молекулярна маса | 152.120115134 г моль−1 |
| Зовнішній вигляд | Білі, напівпрозорі кристали |
| Густина | 0.990 г см−3 |
| Розчинність (вода) | 1.2 г дм−3 |
| Розчинність (ацетон) | ~2500 г дм−3 |
| Розчинність (оцтова кислота) | ~2000 г дм−3 |
| Розчинність (діетилефір) | ~2000 г дм−3 |
| Розчинність (хлороформ) | ~1000 г дм−3 |
| Розчинність (етанол) | ~1000 г дм−3 |
| Тиск насиченої пари | 4 мм рт. ст. (при 70 °C) |
| Оптична активність [α]D | +44.1° |
| Небезпеки | |
| Класифікація ЄС |
|
| R-фрази | R11 R22 R36/37/38 |
| S-фрази | S16 S26 |
| NFPA 704 | |
| Температура спалаху | 64 °C (147 °F) |
| Вибухові границі | 3,5% |
| Пов'язані речовини | |
| Інші (Кетони) | Фенхон, туйон |
| Пов'язані речовини | Камфен, пінен, борнеол, ізоборнеол, камфорсульфонова кислота |
| Якщо не зазначено інше, дані наведено для речовин у стандартному стані (за 25 °C, 100 кПа) | |
| Інструкція з використання шаблону | |
| Примітки картки | |
Ка́мфора — воскоподібна, легкозаймиста, біла або прозора тверда речовина з сильним ароматним запахом. Це терпеноїд з хімічною формулою C10H16O. Вона міститься у деревині камфорного лавра (Cinnamomum camphora), великого вічнозеленого дерева, яке росте в Азії (зокрема, на Суматрі, Борнео і Тайвані), а також борнеокамфорного дерева (Dryobalanops Aromatica), гіганта лісів Борнео. Вона також трапляється у деяких інших споріднених дерев родини лаврових, особливо Ocotea usambarensis. Висушене листя розмарину (Rosmarinus officinalis) з родини Глухокропивових містить до 20% камфори. Її також можна одержати синтетичним шляхом зі скипидару. Вона цінується за її запах, і використовується, як інгредієнт для приготування їжі (в основному в Індії), як рідина для бальзамування, з лікувальною метою, а також у релігійних церемоніях. Основним джерелом камфори в Азії є камфорний базилік.
Норкамфора є похідним камфори з трьома метильними групами, заміненими на водень.
Зміст
Історія
Слово «камфора» походить від французького слова [camphre] помилка: {{lang}}: текст вже має курсивний шрифт (допомога) , а воно, у свою чергу, від середньовічного латинського [camfora] помилка: {{lang}}: текст вже має курсивний шрифт (допомога), у арабській мові — [kafur] помилка: {{lang}}: текст вже має курсивний шрифт (допомога) , у санскриті — karpūra. У кінцевому рахунку термін походить від давньомалайського kapur barus що означає «крейда з Барусу». Барус — назва древнього порту, розташованого недалеко від сучасного міста Сіболга на західному узбережжі острова Суматра (сьогодні провінція Північна Суматра, Індонезія). Цей порт був побудований переважно для Індійсько — Батакської торгівлі камфорою і спеціями. Торговці з Індії, Східної Азії і Близького Сходу використовували термін kapur barus, щоб купувати висушений сік камфорних дерев у місцевих батакських племен. У давній малайсько-австронезійській мові (батакський алфавіт, адаптований з санскриту), він також відомий як [kapur Barus] помилка: {{lang}}: текст вже має курсивний шрифт (допомога). Навіть зараз місцеві племена та індонезійці в цілому асоціюють нафталінові кульки та кульки від молі з [kapur Barus] помилка: {{lang}}: текст вже має курсивний шрифт (допомога). Місцеві племена використовують камфору як дезодорант, засіб для надання блиску дерев'яним виробам, для традиційних ритуалів і як неїстівний консервант, оскільки камфорне дерево є аборигенним видом цього регіону. Дерево під назвою «Kamfer» (індонезійською мовою), також відоме своєю стійкістю до тропічних термітів. [джерело?]
Завдяки здатності камфори до сублімації вона має кілька застосувань. Тривала міжнародна торгівля нею зробила камфору широко відомою по всій Аравії у доісламські часи, вона згадана у Корані (76:5) як ароматизатор для напоїв. У ХІІІ столітті вона використовувалась у рецептах скрізь у мусульманському світі, починаючи з головних страв, таких як tharid і як компонент у десертах.
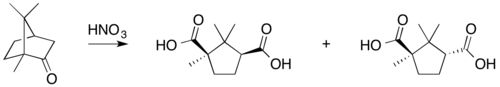
Вже у ХІХ столітті було відомо, що камфора може бути окиснена азотною кислотою до камфорної кислоти. Халлер і Блан опублікували напівсинтез камфори з камфорної кислоти, яка, хоч і продемонструвала свою структуру, але не була досліджена. Уперше закінчений повний синтез камфорної кислоти був опублікований Густавом Комппа у 1903 році. Початковими компонентами були діетилоксалат і 3,3-діметилпентанова кислота, з яких з допомогою конденсації Кляйзена отримали дикетокамфорну кислоту. Метилювання йодистим метилом і складна процедура відновлення дали камфорну кислоту. Вільям Перкін трохи пізніше опублікував інший варіант синтезу. Раніше деякі органічні сполуки (наприклад, сечовина) були синтезовані у лабораторії як доказ концепції, але камфора була обмеженим природним продуктом зі світовим попитом. Комппа зрозумів це і почав промислове виробництво камфори в Тайніонкоскі, Фінляндія, в 1907 році.
Виробництво
Камфора може бути отримана з альфа-пінену, якого є багато в оліях хвойних дерев, і шляхом перегонки зі скипидару, отриманого як побічний продукт хімічної обробки целюлози. З використанням оцтової кислоти як розчинника і сильної кислоти як каталізатора, альфа-пінен легко перебудовується у камфен, який у свою чергу через перегрупування Вагнера-Меєрвейна перетворюється в ізоборніл катіон, який захоплюється ацетатом, після чого утворюється ізоборнілацетат. Гідроліз до ізоборнеолу з подальшим окисненням дає рацемічну камфору.
На противагу цьому, у природі камфора зустрічається у вигляді D-енантіомеру.
Біосинтез
У біосинтезі камфору отримують з гераніл пірофосфату за допомогою циклізації ліналоіл пірофосфату до борніл пірофосфату, з подальшим гідролізом до борнеолу і окисненням до камфори.
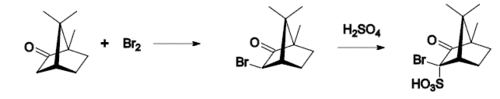
Реакції
Типові реакції камфори
- бромування,
- окиснення азотною кислотою
- перетворення в ізонітрозокамфору.
Камфора також може бути приведена до ізоборнеолу з допомогою боргідриду натрію.
У 1998 році К. Чакрабарті з колегами з Indian Association for the Cultivation of Science у Калькутті виготовили тонку алмазну плівку з використанням камфори як прекурсора для хімічного осадження з парової фази.
У 2007 році були успішно синтезовані вуглецеві нанотрубки з використанням камфори у процесі хімічного осадження з парової фази.
Використання
Сучасні області застосування включають камфору як пластифікатор для нітроцелюлози (див. целулоїд), як репелент проти молі, як антимікробну речовину, у бальзамуванні й у феєрверках. Тверда камфора випускає пари, які утворюють антикорозійне покриття, і тому її кладуть у скрині з інструментами для захисту від корозії.
Кристали камфори використовуються для запобігання пошкодженню колекцій комах іншими дрібними комахами, а також як супресивний засіб проти кашлю. Згідно з деякими народними рецептами, камфора відлякує змій та інших рептилій своїм сильним запахом. Аналогічно камфора, як вважають, є токсичною для комах і, таким чином, іноді використовується як репелент.
Кулінарія
У стародавній і середньовічній Європі камфора використовувалась як інгредієнт у солодощах. Вона входила до складу найрізноманітніших солодких і солоних страв у середньовічних кулінарних книгах арабською мовою, таких як al-Kitab al-Ṭabikh, укладена Сайяр ібн аль-Варраком у Х столітті, і Андалузька кулінарна книга невідомого автора ХІІІ століття. Вона також з'являється у солодких і солоних стравах у книзі Ni'matnama, написаній наприкінці 15 століття для султанів міста Манду.
Нині камфора використовується як ароматизатор в Азії, в основному для солодощів. Вона широко використовується в кулінарії, переважно для десертних страв у Індії, де вона відома як kachha karpooram або «pachha karpoora» («сира / необроблена камфора»), мовою телугу: (పచ్చ కర్పూర), тамільською мовою: (பச்சைக் கற்பூரம்), мовою каннада:(ಪಚ್ಚ ಕರ್ಪೂರ) і наявна в індійських магазинах, де вона позначена як «їстівна камфора». Ароматизовані камфорні таблетки також використовуються як дезодоруючий елемент і зберігаються в одязі, призначеному для особливих випадків і фестивалів, а також у кутках шаф як репелент проти тарганів.
Медичне застосування
Камфора легко всмоктується через шкіру і викликає відчуття охолодження аналогічно до ментолу, діє як легкий місцевий анестетик і протимікробний засіб. Існують гелі проти свербіння та охолоджувальні гелі з камфорою як активним інгредієнтом. Камфора є активним інгредієнтом (разом з ментолом) у комбінованих препаратах, таких як ВІК ВапоРаб.
Камфора може також бути застосована перорально у невеликих кількостях (50 мг) при незначних серцевих симптомах і втомі. Протягом більшої частини 1900-х років такий препарат продавався під торговою назвою Musterole; виробництво припинилося в 1990 році.
Камфора використовувалась у стародавній Суматрі для лікування розтягнень, набряків і запалень. Камфора є компонентом болезаспокійливої камфорної настоянки опіуму з XVIII століття. Також у XVIII столітті камфора була використана Ауенбруггером в лікуванні манії. На підставі праць Ганемана, камфора, (розчинена у спирті) була також успішно використана для боротьби з епідемією холери 1854–1855 років у Неаполі.
Травознавство
Камфора доступна як ефірна олія для ароматерапії або точкової аплікації.
Індуїстські релігійні церемонії
Камфора широко використовується в індуїстських релігійних церемоніях. Індуси вшановують священне полум'я шляхом спалювання камфори, що є важливою складовою частиною багатьох релігійних церемоній. Камфора використовується на святі Махашиватрі на честь Шиви, індуїстського бога руйнування і (від)творення. Як природна смолиста речовина, вона горить холодним полум'ям, не залишаючи попелу, що символізує свідомість. Більшість храмів на півдні Індії припинили спалювання камфори усередині храмів через сильний нагар, який вона створює, проте її досі спалюють на відкритих майданчиках.
У штатах Таміл-Наду, Андхра-Прадеш, Карнатака, Керала і Андаманських островах камфора є основним інгредієнтом у будь-якому священному ритуалі. Наприкінці священного ритуалу, який має назву Аарті (або Араті), полум'я камфори запалюється для вшанування божеств.
У індуїстських церемоніях пуджа камфора спалюється у церемоніальній ложці для здійснення ритуалу аарті. Цей тип камфори, оброблений білий кристалічний різновид, також продається в індійських продуктових магазинах. Він не підходить для приготування їжі і є небезпечним для здоров'я, якщо його з'їсти.
Вплив на організм
Камфора має ефект, аналогічний до дії агоністів мускаринових рецепторів.
Малі дози
Її вплив на організм включає: тахікардію, вазодилатацію шкірних судин (почервоніння) сповільнене дихання, зниження апетиту, підвищення секреції і екскреції, наприклад, потовиділення і діурезу.
Токсичність великих доз
Камфора є отруйною у великих дозах. Вона спричиняє такі симптоми, як дратівливість, дезорієнтація, млявість, м'язові спазми, блювання, біль у животі, судоми і напади. Летальна доза для дорослих знаходиться у діапазоні 50-500 мг / кг (перорально). Як правило, два грами призводять до серйозного отруєння, і чотири грами є потенційно смертельними.
Регулювання
У 1980 році Адміністрація з контролю якості харчових продуктів і ліків США (FDA) встановила припустимий ліміт вмісту камфори в споживчих товарах 11%, і повністю заборонила продукти, позначені як камфорна олія і камфорна мазь (крім «білої камфорної ефірної олії», яка не містить значної кількості камфори). Оскільки існують альтернативні методи лікування, медичне використання камфори не вітається FDA, за винятком нанесення на шкіру (лікарські порошки, які містять лише невелику кількість камфори).
Див. також
Література
- Фармацевтична хімія : [арх. 11 березня 2021] : підручник / ред. П. О. Безуглий. — Вінниця : Нова Книга, 2008. — 560 с. — ISBN 978-966-382-113-9. (С.209-212)
Посилання
- КАМФОРА РАЦЕМІЧНА [Архівовано 14 березня 2016 у Wayback Machine.] //Фармацевтична енциклопедія
- Camphor Evidence-based Monograph from Natural Medicines Comprehensive Database
- INCHEM [Архівовано 11 лютого 2021 у Wayback Machine.] at IPCS (International Programme on Chemical Safety)