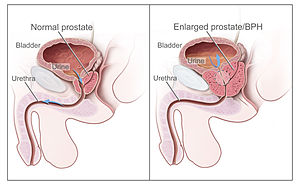
Доброякісна гіперплазія передміхурової залози
| Доброякісна гіперплазія передміхурової залози | |
|---|---|
|
Нормальна (зліва) і патологічно збільшена (справа) передміхурова залоза
| |
| Спеціальність | урологія |
| Препарати | фінастерид, тамсулозин, празозин, теразозин, Лейпрорелін, доксазозин, дутастерид, тадалафіл, альфузозин, альфузозин, тадалафіл, фінастерид, доксазозин і indoramind |
| Класифікація та зовнішні ресурси | |
| МКХ-11 | GA90 |
| МКХ-10 | N40 |
| OMIM | 600082 |
| DiseasesDB | 10797 |
| MedlinePlus | 000381 |
| eMedicine | med/1919 |
| MeSH | D011470 |
| | |

| 1.Сечовий міхур 2.Тазова кістка 3.Пеніс 4.Кавернозне (печеристе) тіло пенісу 5.Головка пенісу 6.Крайня плоть 7.Отвір уретри 8.Товста кишка 9.Пряма кишка | 10.Сім’яні міхурці 11.Сім’явиносна протока 12.Передміхурова залоза 13.Бульбоуретральна залоза 14.Анус 15.Сім’яна судина 16.Придаток яєчка 17.Яєчко 18.Калитка (Мошонка) |
Доброякісна гіперплазія передміхурової залози (Доброякісна гіперплазія простати, Аденома передміхурової залози, Аденома простати, ДГПЗ) — це захворювання, що супроводжується розростанням тканин залозистого епітелію передміхурової залози, які оточують сечовипускний канал, що призводить до порушення сечопуску. Найчастіше при виникненні доброякісної гіперплазії передміхурової залози розростання тканин проходить у вигляді утворення одного або кількох вузлів, які поступово ростуть і здавлюють сечовипускний канал, що призводить до утруднення сечовиділення. Пухлиноподібний ріст при доброякісній гіперплазії простати має доброякісний характер, та не спроводжується метастазуванням, що відрізняє його від злоякісної пухлини передміхурової залози.
Зміст
Епідеміологія
Згідно оцінки кількості хворих на доброякісну гіперплазію передміхурової залози, дане захворювання є найбільш поширеною патологією сечостатевої системи у чоловіків віком більш ніж 50 років. За даними клінічних досліджень, доброякісна гіперплазія простати діагностується у 11,3 % чоловіків у віці 40—49 років, у віці від 50 років частота гіперплазії простати зростає до 25 %, у віці 60-70 років частоту даного захворювання оцінюють у 50 %, у віці 90 років частота доброякісної гіперплазії становить близько 90 %. За даними Інституту урології НАМН України, поширеність доброякісної гіперплазії простати в Україні у 2013 році становила 1132,9 на 100 тисяч дорослого чоловічого населення, у тому числі серед чоловіків віком 50–60 років дану патологію виявлено у близько 20 %, 60–70 років — у 75 %, 90 років — у 88 % випадків осіб даного віку. У осіб пенсійного віку (більше 60 років) цей показник становить 4434,5 на 100 тисяч чоловічого населення даного віку.
Етіологія і патогенез
Тривалий час основним етіологічним фактором розвитку доброякісної гіперплазії передміхурової залози вважалось вікове зниження вироблення тестостерону статевими залозами чоловіків та підвищення на цьому фоні перетворення його у дигідротестостерон під впливом ферменту 5-альфа-редуктази. Унаслідок цього у простаті накопичується активніший гормон дигідротестостерон, збільшення кількості якого призводить до стимуляції росту епітеліальних клітин передміхурової залози. Одночасно також підвищується активність ферменту ароматази в стромальних клітинах простати, що також стимулює ріст стромальних клітин залози. Одночасно також активуються альфа-адренорептори та М-холінорецептори, що призводить до прогресування явищ обструкції в нижніх відділах сечових шляхів, а також появи симптомів подразнення нижніх сечових шляхів, які в сумі й складають клінічну картину доброякісної гіперплазії передміхурової залози. Проте дослідження останніх десятиліть виявляють зміни в розумінні патогенезу формування доброякісної гіперплазії передміхурової залози. Згідно досліджень останніх десятиліть, значну роль у розвитку гіперплазії простати грає співвідношення в її структурі епітелію та строми, а також продукція факторів росту, які регулюють це відношення. Ще у 1925 році Райшауер висловив припущення, що аденома простати розвивається із периуретральних фібром'язових вузлів. У подальших дослідженнях у 1970 році встановлено, що клітини епітелію не можуть ділитися при відсутності клітин строми. Також у ці роки встановлено, що чоловічі статеві гормони не впливають безпосередньо на поділ клітин простати. У 1976 році вперше виділено фактори росту із тканини раку простати, а за кілька років фактори росту виділені також і з клітин гіперплазованої простати, а пізніше і з клітин здорової простати. У ці ж роки вперше висловлено думку про те, що доброякісна гіперплазія передміхурової залози виникає унаслідок стимуляції поділу фібробластів епітеліальним фактором росту. Одночасно виникла теорія про те, що доброякісна гіперплазія простати є одним із асоційованим із старінням захворювань, які обумовлені віковим гормональним дисбалансом, і є якби побічним наслідком закладеної у генах програми онтогенезу людини. Встановлено також, що ризик розвитку доброякісної гіперплазії передміхурової залози збільшується у випадку супутніх запальних захворювань простати. Пізніші дослідження встановили також зв'язок розвитку доброякісної гіперплазії простати з дефіцитом вітаміну D, вікового дефіциту дегідроепіандростерону і прогестерону, дефіциту мелатоніну, дефіциту серотоніну, вазопресину, а також появи інсулінорезистентності. Встановлено також, що сексуальна активність чоловіків не впливає на частоту виникнення гіперплазії передміхурової залози, проте кастрація запобігає виникненню як гіперплазії простати, так і раку простати. Не встановлено зв'язок розвитку аденоми передміхурової залози із перенесеними венеричними захворюваннями, вживанням алкоголю та тютюну, а також сексуальною орієнтацією.
Сучасна теорія патогенезу доброякісної гіперплазії передміхурової залози головним фактором виникнення захворювання вважає порушення балансу між факторами росту епітеліальної тканини простати (епідрермального фактора росту і кератиноцитний фактор росту) та стромальної частини простати (фібробластиний фактор росту-2), а також з іншого боку трансформуючим фактором росту β, який пригнічує ріст клітин простати. Це порушення виникає на фоні порушення гормональної регуляції простати, зокрема зниженням вироблення андрогенів. Порушення гормональної регуляції призводить до переважання росту строми простати, та виникнення доброякісної гіперплазії простати. Іншим вагомим чинником виникнення доброякісної гіперплазії простати вважається мікротравматизація периуретрально розташованих клітин простати (що відбувається при сечовипуску, еякуляції, інфекціях передміхурової залози). Це призводить до підвищення вивільнення фібробластного фактору росту, що є частиною процесу відновлення пошкодженої тканини та сприяє розвитку гіперплазії строми, а в подальшому до активації синтезу кератиноцитного фактору росту, та стимуляції мітозу клітини епітелію простати. Одночасно у хворих формуються вікові зміни м'язів шийки сечового міхура, що призводить до спазмування шийки сечового міхура, а також порушення роботи детрузора сечового міхура. Цьому сприяє активація альфа-адренорецепторів, особливо у шийці сечового міхура, що призводить до спазмування шийки сечового міхура та погіршення сечопуску. Вузли гіперплазії на передміхуровій залозі також погіршують кровопостачання шийки сечового міхура та задньої стінки уретри, що також сприяє виникненню дисфункції детрузора сечового міхура. Одночасно спостерігається також зниження кількості М-холінорецепторів у стінці сечового міхура на фоні його ультраструктурних змін, що є ознакою значної гіпоксії тканин сечового міхура, й також сприяє виникненню затримки сечі. Одночасно спостерігаються мікротравми стінок сечового міхура, зумовлені його перерозтягненням, що призводить до вивільнення факторів росту клітин, наслідком чого стає поява грубих змін стінки сечового міхура — значне збільшенню маси детрузора, зростання кількості колагену у стінці, у подальшому також виникають вторинні порушення кровопостачання та іннервації. Наслідком цих процесів стає погіршення скорочення детрузора, зменшення його пластичності, появи гіперчутливості міхура. Усі перераховані факти дають можливість зробити висновок, що патогенез доброякісної гіперплазії передміхурової залози пов'язаний не лише із гіпертрофією самої простати, але й із механічною обструкцією шийки сечового міхура, порушенням скорочення гладких м'язів шийки міхура та порушенням скорочення детрузора сечового міхура. Усі ці фактори можуть виникати незалежно один від одного, а в сумі вони призводять до виникнення клінічної картини доброякісної гіперплазії простати.
Класифікація
Доброякісна гіперплазія передміхурової залози класифікується за морфологічною формою, конфігурацією, напрямком росту пухлини, розмірами та ступенем порушення скоротливої здатності сечового міхура.
За морфологією гіперплазія передміхурової залози поділяється за співвідношенням у її структурі епітеліальних, сполучнотканинних та м'язових елементів на залозисту, міоматозну, фіброзну та змішану форми захворювання.
За конфігурацією доброякісна гіперплазія передміхурової залози поділяється на аденому однієї середньої долі, двобічну (з двох бокових долей), із трьох долей, а також гроноподібну (складається із великої кількості дольок).
За напрямком росту доброякісна гіперплазія передміхурової залози поділяється на внутрішньоміхурну форму, коли аденома росте через уретру в порожнину сечового міхура, спричинюючи деформацію його внутрішнього сфінктера, наслідком чого є порушення сечовиділення; підміхурову форму, коли аденома росте в напрямку до прямої кишки, чим спричинює порушення діяльності простатичної частини уретри, що сприяє накопиченню в сечовому міхурі великої кількості залишкової сечі, що в подальшому спричинює перерозтягнення сечового міхура; та ретротригональну форму, коли аденома розміщується під сечоміхуровим трикутником, що спричинює перетискування сечоводів із їх подальшим розширенням, і подальшим погіршенням відтоку сечі із сечового міхура із формуванням гіпертрофії детрузора сечового міхура із подальшим формуванням атонії стінки сечового міхура.
За розмірами доброякісна гіперплазія передміхурової залози поділяється на малу (до 25 см³), середню (25—80 см³), велику (80—250 см³) і гігантську (більш ніж 250 см³).
За ступенем порушення скоротливої здатності сечового міхура доброякісна гіперплазія передміхурової залози поділяється на три стадії:
- І стадія. Компенсована стадія, яка характеризується мінімальними об'єктивними проявами хвороби, сечовий міхур спорожнюється повністю, відсутні симптоми порушення функції верхніх відділів сечовивідних шляхів.
- ІІ стадія. Стадія субкомпенсації, при якій спостерігається виявлення залишкової сечі в сечовому міхурі (початково до 100 мл, пізніше більше), поступово розвиваєеться міхурово-сечоводний рефлюкс та дилятація верхніх відділів сечовивідних шляхів, при подальшому обстеженні спостерігаються симптоми пієлонефриту та латентної стадії хронічної ниркової недостатності.
- ІІІ стадія. Стадія декомпенсації, при якій спостерігається виникнення парадоксальної ішурії та посилення явищ ниркової недостатності, у тому числі симптомами анемії та схудненням.
Клінічна симптоматика
Клінічні симптоми доброякісної гіперплазії передміхурової залози різноманітні, більшість із них поділяються на обструктивні та іритативні. До обструктивних симптомів відносяться затруднення сечопуску, відчуття неповного спорожнення сечового міхура, несвоєчасний початок сечопуску, натужування під час сечопуску, послаблення та переривання струменя сечі. До іритативних симптомів відносяться почащений сечопуск, імперативний позив до сечопуску, симптоми імперативного нетримання сечі (відчуття неповного спорожнення сечового міхура і підтікання сечі відразу після сечовипускання). Симптоми доброякісної гіпертрофії простати наростають поступово, та прогресують протягом кількох років у залежності від ступеню розвитку захворювання.
Першими симптомами доброякісної гіперплазії передміхурової залози є незначні порушення сечопуску: затруднення і запізнення виділення струменю сечі, в'ялий струмінь сечі, поява імперативних позивів до сечопуску, відчуття неповного спорожнення сечового міхура, а також збільшення частоти сечопуску в нічний час. У наступній стадії захворювання хворі скаржаться на переривистий та багатофазний сечопуск, із фазами перерви навіть до кількох хвилин, для проведення повноцінного акту сечопуску хворі вимушені напружувати м'язи черевного пресу, сеча у зв'язку із затримкою в сечовому міхурі стає мутною, іноді із домішкою крові (унаслідок формування каменів у сечовому міхурі), спостерігається також нетримання сечі. У цей період у хворих може спостерігатися також гостра затримка сечі із необхідністю катетеризації сечового міхура, в них також з'являються ознаки супутнього пієлонефриту та перші ознаки ниркової недостатності — сухість і гіркота в роті, спрага, поліурія. У стадії декомпенсації у хворих іноді візуально можна побачити випинання переповненого сечового міхура на передній черевній стінці. Хворі у цій стадії відчувають періоди як денного, так і нічного самовільного виділення сечі по краплях, спостерігається також парадоксальна ішурія — поєднання затримки сечовиділення із її нетриманням. Одночасно у хворих наростають симптоми супутнього пієлонефриту та ниркової недостатності, у хворих постійно відчувається сухість і гіркома в роті, загальна слабкість, похудіння, з'являються явища анемії. У хворих спостерігається запах сечі як від шкіри, так і у повітрі, яке вони видихають. При прогресуванні явищ ниркової недостатності та порушенні водно-електролітного балансу хворі помирають від наростання явищ уремії.
Діагностика
Діагностика доброякісної гіперплазії передміхурової залози розпочинається вже від правильного збору анамнезу захворювання та оцінки скарг хворого. Для цього часто застососовуються опитувальні листи анкетної форми, які зазвичай включають 7 запитань. Відповіді на ці запитання у балах дають лікарю попередню оцінку вираженості симптомів захворювання з точки зору самого хворого. Важливим методом діагностики залишається пальцеве ректальне обстеження простати як найпростіший та найдоступніший, хоча й менш інформативний спосіб диференціальної діагностики ДГПЗ і раку простати, який допомає оцінити щільність залози, ступінь та напрям її збільшення, виявити її болючість та оцінити рухливість прилеглих органів. Для обстеження застосовуються також загальний аналіз крові та загальний аналіз сечі, біохімічний аналіз крові з обов'язковим визначенням рівня креатиніну і сечовини крові. Важливе місце займає також визначення простат-специфічного антигена, який зазвичай підвищується при наявності гіперплазії передміхурової залози, проте також підвищується і при раку простати. Серед інших способів діагностики гіперплазії передміхурової залози застосовуються ультразвукове обстеження передміхурової залози (у тому числі трансректальне), уродинамічне обстеження (визначення швидкості потоку сечі, часу сечопуску), рентгенологічне обстеження органів сечостатевої системи (у тому числі із застосуванням рентгенконтрастних препаратів, а за необхідності й застосування комп'ютерної томографії). За неможливості встановлення діагнозу стандартними методами застосовуються також ендоскопічні методи (цистоскопія, уретроскопія), а також застосовується біопсія тканини простати.
- Гістологічна структура простати
Лікування
У лікуванні хворих доброякісною гіперплазією передміхурової залози застосовуються медикаментозне та оперативне лікування.
У медикаментозному лікуванні доброякісної гіперплазії простати застосовуються препарати групи альфа-адреноблокаторів. Вони поділяються на неселективні (діють як на гладенькі м'язи простати і сечового міхура), так і на адренорецептори в серцево-судинній системі та інших системах організму, та селективні, які діють виключно на адренорецептори сечовидільних шляхів. До перших відносяться празозин, доксазозин і теразозин; до селективних препаратів відносяться альфузозин і тамсулозин. У лікуванні доброякісної гіпертрофії передміхурової залози застосовуються також інгібітори 5-альфа-редуктази. До синтетичних препаратів цієї групи відноситься фінастерид і дутастерид. Природними препаратами групи інгібіторів 5-альфа-редуктази є екстракт із пальми Сереноа та екстракт кори африканської сливи. У медикаментозному лікуванні гіперплазії передміхурової залози застосовуються також блокатори М-холінорецепторів, зокрема оксибутинін, толтеродин і соліфенацин; а також інгібітори фосфодіестерази 5 типу (по типу силденафіла).
Найрозповсюдженішим способом оперативного лікування доброякісної гіперплазії передміхурової залози є трансуретральна резекція передміхурової залози. Операція виконується шляхом введення через уретру до простати спеціального інструмента (резектоскопа), після чого за допомогою спеціальної петлі проводиться електрична резекція тканини простати, яка пізніше вимивається через сечовий міхур. Для лікування запущених випадків аденоми простати застосовується трансвезикальна аденектомія, яка виконується розрізом через сечовий міхур, при якій видаляється уся тканина передміхурової залози. Іноді простатектомія виконується розрізом із прямої кишки. Також за необхідності в запущеній стадії захворювання можуть проводитись паліативні операції: кріодеструкція передміхурової залози, епіцистостомія та троакарна цистостомія, які застосовуються для швидкого налагодження відтоку сечі. Іншими методами лікування доброякісної гіперплазії передміхурової залози є установка простатичного стента в місці звуження сечовидільного каналу, балонна дилятація простати, ультразвукова та гольчата абляція тканини простати. Новітнім методом лікування доброякісної гіперплазії простати є емболізація артерій простати шляхом введення до артерій простати спеціального препарату, який перекриває просвіт судини, що призводить до втрати живлення тканини простати. та її зменшення.
Посилання
- Что такое аденома простаты [Архівовано 26 листопада 2020 у Wayback Machine.] (рос.)
- АДЕНОМА ПРОСТАТЫ [Архівовано 4 серпня 2018 у Wayback Machine.] (рос.)
- АДЕНОМА ПРОСТАТЫ [Архівовано 13 липня 2020 у Wayback Machine.] (рос.)
- Доброякісна гіперплазія передміхурової залози
- Как лечить аденому простаты [Архівовано 10 серпня 2018 у Wayback Machine.] (рос.)
- Доброякісна гіперплазія передміхурової залози
|