
Спутник V
| Спутник V | |
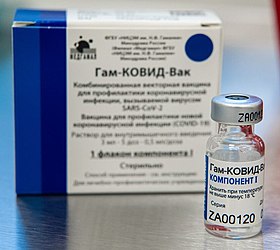 | |
| Прізвисько | Spoetnik V, Sputnik V, Спутник V, Szputnyik vakcina, Spoutnik V і Sputnik V |
|---|---|
| Названо на честь | Перший штучний супутник Землі і перемога |
| Країна походження |
|
| Є вакциною проти | коронавірусна хвороба 2019 (COVID-19) |
| Спосіб введення препарату | внутрішньом’язова ін’єкція |
| Розробник | Науково-дослідний інститут епідеміології та мікробіології ім. Н. Ф. Гамалії |
| Дата анонсу | травень 2020 |
| Ціна | 20 $ і 10 $ |
| Кількість підписників у соціальних мережах | 1 017 456 |
| Офіційний сайт(англ.)(рос.)(араб.)(кит.)(ісп.)(порт.)(фр.) | |
| | |
Гам-КОВІД-Вак (рос. Гам-КОВИД-Вак — реєстраційне найменування; лат. Gam-COVID-Vak), торгова марка «Спутник V» (вимова рос. [спу́тнік ві], V — скорочення від англ. victory, перемога) — вакцина, що за даними розробників має діяти проти COVID-19. Створена російським Національним дослідницьким центром епідеміології та мікробіології ім. Гамалії. Схвалена до використання у 51 країні світу; заборонена в Україні.
5 грудня 2020 року в Росії почалася масова вакцинація від коронавірусу цієї вакциною. Дані щодо самої вакцини та результати випробування піддавалися критиці деякими західними спеціалістами — зокрема, через непрозорість процесу розробки вакцини та швидке її затвердження російським урядом.
Станом на літо 2021 вакцину зареєстрували лише в 59 країнах, які здебільшого були союзниками СРСР або набули союзних відносин з РФ. Домовлені постачання в ряд таких країн РФ не змогла виконати, що призвело до тяганини з повернення завдатків, репутаційних збитків, протестів в окремих країнах щодо невдалого вибору постачальника вакцини.
Зміст
Загальний опис
Вакцина являє собою вірусну векторну вакцину на основі аденовірусу людини, який містить у своєму геномі вставку, що кодує фрагмент S-білка SARS-CoV-2, і викликає імунну відповідь. Вакцину розробив колектив лабораторії клітинної мікробіології відділу медичної мікробіології НДЦЕМ ім. М. Ф. Гамалії МОЗ РФ під керівництвом доктора медичних наук, члена-кореспондента РАН Д. Ю. Логунова, який розробляв також вакцини проти вірусів Ебола і MERS.
Вакцина є двокомпонентною: використано два рекомбінантних аденовірусних векторів на основі аденовірусу людини 26 серотипу (Ad26, «компонент I») і 5 серотипу (Ad5, «компонент II»), модифіковані біотехнологічним способом (містять ген S-білка вірусу SARS-CoV-2). Компоненти вакцини вводяться внутрішньом'язово, у два етапи з інтервалом у 3 тижні.
Історія
У травні 2020 року Національний центр епідеміологічних та мікробіологічних досліджень оголосив про розробку вакцини, яка не має серйозних побічних ефектів. До серпня 2020 року були закінчені два клінічних випробування першої та другої фази, з участю по 38 випробовуваних в кожному. Лише в одному з досліджень використовувалася форма вакцини, що пізніше отримала реєстрацію на «обмежених умовах». Згідно з планом, 9 пацієнтів отримали один компонент, 9 пацієнтів — другий компонент, і 20 осіб — обидва компоненти вакцини.
Вакцина зареєстрована умовно, згідно з прийнятим Урядом Російської Федерації порядком доступу на ринок препаратів, призначених для профілактики COVID-19. Відповідне реєстраційне посвідчення було видано 11 серпня МОЗ Росії.
Початок досліджень третьої фази, в яких буде брати участь кілька десятків тисяч осіб, очікується не пізніше 26 серпня. Відповідно до особливих умов прискореної реєстрації та інструкції до вакцини, кожне застосування вакцини повинно відстежуватися в федеральному регістрі.
Початок промислового виробництва вакцини планується на вересень 2020 року. До кінця 2020 року власне виробництво Гамалії, згідно з інтерв'ю іноземному виданню, планується вивести на виробничу потужність 3-5 млн доз на рік. За даними російських «ЗМІ», до 15 серпня відбувся запуск виробництва; три підприємства зможуть випускати близько мільйона доз на місяць на кожному з потенційним подвоєнням потужностей до зими.
Через початок масової вакцинації у грудні 2020 року МОЗ РФ вирішили припинити набір добровольців у групу плацебо, оскільки деякі учасники дослідження щепилися самою вакциною, дізнавшись, що їм вводили плацебо. На думку виконавчого директора Асоціації організації з клінічних досліджень Світлани Завідової, після втрати групи плацебо дослідження можна вважати проваленим.
2021
У березні швейцарська фармацевтична компанія «Adienne» заявила, що вироблятиме вакцину в Італії, підписавши з Фондом національного добробуту РФ відповідну угоду. У квітні Словаччина оголосила, що партія вакцини «Супутник V», отримана від Росії, є іншим препаратом, а не тим, який хвалили в журналі «The Lancet».
З листопада США закрили кордон для туристів, вакцинованих «Супутником V».
Ефективність і безпека
Оцінка ефективності вакцини проводилася за допомогою спеціально розробленого тесту, що визначає рівень антитіл до вірусного білка, а не звичайним методом, коли пацієнт після введення вакцини чекає зараження. За твердженням генерального директора РФПІ К. О. Дмитрієва такий тест підтверджує працездатність вакцини.
У звіті НДЦЕМ імені Гамалії вказується про проведення досліду над 38 здоровими добровольцями обох статей у віці від 18 до 60 років. У результаті спостереження протягом 42 днів з моменту введення вакцини у всіх піддослідних було виявлено «утворення вірусо-нейтралізуючих антитіл до вірусу SARS-CoV-2». Разом з тим зазначається, що у добровольців спостерігалося 144 побічних ефекти, 31 з яких не завершилося на момент закінчення випробувань. Побічні ефекти в основному легкого або середнього ступеня вираженості: підвищення температури, біль у місці введення, висип. Також у звіті наголошується, що «Захисний титр в цей час невідомий. Тривалість захисту невідома. Клінічні дослідження з вивчення епідеміологічної ефективності не проводилися».
В Росії спостерігаються часті випадки зараження коронавірусом відразу після вакцинації, частина із них летальні[неавторитетне джерело]. 58 % росіян не готові робити щеплення російською вакциною.
Міжнародний інтерес
За заявою генерального директора РФПІ К. О. Дмитрієва, фонд отримав попередні заявки на купівлю 1 млрд доз вакцини з 20 країн, і крім того, РФПІ домовився про виробництво вакцини в п'яти країнах, але ці дані не були підтверджено.
У РФПІ заявляють про намір провести клінічні випробування вакцини в ряді країн, крім Росії.
Попередня домовленість про виробництво вакцини за кордоном досягнута з Бразилією. Бразильське Національне агентство з санітарного нагляду не схвалило до використання «Спутник V».
Російська вакцина зареєстрована в Росії, Білорусі, Аргентині, Болівії, Сербії, Алжирі, Палестині, Венесуелі, Парагваї, Туркменістані, ОАЕ, Ірані, Гвінеї, Тунісі, Вірменії, Мексиці, Угорщині, Нікарагуа. Туреччина станом на 21 січня 2021 року тимчасово відмовилася від її купівлі. Міністр охорони здоров'я Туреччини зазначив, що вакцина станом січень 2021 не може отримати ліцензію через невідповідність належній лабораторній практиці.
Критика
Голова відділення лабораторної медицини Каролінського інституту Матті Сельберг зазначає, що мале число учасників клінічного випробування, в якому були об'єднані перша і друга фази, не дозволяє судити про відсутність побічних ефектів при масовому застосуванні вакцини, однак, самі розробники вакцини вважають її надійною, оскільки вона була розроблена на наявній і добре випробуваній платформі. Також існують побоювання, побічні ефекти від раніше широко не застосованих живих вакцин на базі генно-інженерних вірусів, що можуть залишатися невивченими. Кілька попередніх розробок вакцини на основі вірусу Ad5 були неуспішними; лише одна вакцина на основі Ad5 була схвалена в Китаї для екстреного використання для людей.
Більшість російських медиків, опитаних сервісом «Довідник лікаря», заявили в опитуванні, що не готові зробити щеплення Гам-КОВИД-Вак. З понад 3000 учасників дослідження негативно на це питання відповіли 52 %, згодні на вакцинацію 24,5 %. Понад 66 % респондентів заявили про недостатність даних щодо ефективності вакцини.
Через відсутність наукових публікацій про вакцину у міжнародної спільноти немає правдивої інформації про ефективність? Гам-КОВИД-Вак. В наукових журналах відсутні публікації про випробування вакцини на тваринах, тому немає ніякої можливості оцінити її працездатність на людях.
Скандали
- Словацький державний інститут контролю за лікарськими засобами дослідив зразки вакцини, 2 млн доз якої було закуплено урядом Словаччини, і виявив, що вони не ідентичні тим, що отримали схвальні висновки в публікації авторитетного журналу «The Lancet». Також інститут зазначив, що вони не такі самі, як ті, що використовуються в інших країнах. Про це повідомила 7 квітня 2021 року «Європейська правда», з посиланням на публікацію в словацькому виданні «DennikN».
Див. також
Посилання
- ГРЛС, ЛП-006395 [Архівовано 19 серпня 2020 у Wayback Machine.] 11.08.2020-01.01.2021, Нормативна документація ЛП-006395-110820 [Архівовано 3 березня 2021 у Wayback Machine.]
- Действующая (со всеми внесёнными изменениями) инструкция к вакцине «Гам-КОВИД-Вак» [Архівовано 28 грудня 2020 у Wayback Machine.] — документ на сайті Росздравнадзора.
- Спутник V. sputnikvaccine.com (рос.). Российский фонд прямых инвестиций. Архів оригіналу за 23 серпня 2020. Процитовано 22 серпня 2020. — сайт посвящённый вакцине.
- Наталья Телегина, Елена Виноградова (08.10.2020). Эликсир молодости, нановакцины и «Кагоцел»: над чем прежде работали учёные, создавшие для Путина «Спутник V». Открытые Медиа. Архів оригіналу за 7 липня 2021. Процитовано 12 липня 2021.
|