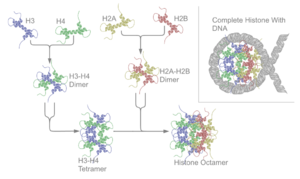
Гістони
| Гістон | Молекулярна маса | Кількість амінокислотних залишків | Вміст основних амінокислот (% від загальної кількості амінокислот) | |
|---|---|---|---|---|
| Лізин | Аргінін | |||
| H1* | 21 130 | 223 | 29,5 | 11,3 |
| H2A* | 13 960 | 129 | 10,9 | 19,3 |
| H2B* | 13 774 | 125 | 16,0 | 16,4 |
| H3 | 15 273 | 135 | 19,6 | 13,3 |
| H4 | 11 236 | 102 | 10,8 | 13,7 |
| *Розміри дещо різні в залежності від виду, дані наведені для бичачих білків | ||||
Гісто́ни — основний клас білків, необхідних для упакування молекул ДНК у хроматин. Гістони мають невелику молекулярну масу (від 11 до 21 кДа) і дуже багаті на основні амінокислоти (аргінін і лізин), завдяки чому взаємодія між гістонами і ДНК стабілізується іонними зв'язками. Для всіх гістонів характерна наявність спільного структурного мотиву, представленого трьома α-спіралями, об'єднаними двома петлями. У більшості клітин маса гістонів приблизно рівна масі ДНК, а їх кількість сягає близько 60 млн. В еукаріотів гістони локалізуються в клітинному ядрі, в архей типу Euarchaeota — у цитоплазмі. У компактизації ДНК решти архей і бактерій можуть брати гістоноподібні білки, проте справжніх гістонів у них немає. Проте у великих ДНК-вмісних вірусів таких як Marseilleviridae присутні гістони.
Білки-гістони були відкриті 1884 року Альбрехтом Косселем у екстрактах ядер еритроцитів птахів. До 40-их років XX століття багато дослідників вважали саме їх носіями спадкової інформації.
У еукаріот існує п'ять різних типів гістонів, а саме H1, H2A, H2B, H3 та H4. Послідовність амінокислот у цих білках мало відрізняється серед еукаріотів різного рівня організації. Найбільш консервативною вона є у гістонів H3 і H4: так гістони H4 корови і гороху відрізняються тільки двома із 102 амінокислотних залишків, а людини і дріжджів — вісьмома, дещо більше різняться між видами еукаріот послідовності гістонів H1, H2A і H2B. Така консервативність їхньої структури свідчить про виняткову важливість для організму, а також про те, що майже кожен амінокислотний залишок у складі цих білки є функціонально важливим. Ця гіпотеза була перевірена на клітинах дріжджів, шляхом заміни нормальних генів гістонів на мутовані. З'ясувалось, що більшість змін в амінокислотній послідовності гістонів є летальною, а та невелика частка мутацій, які не були смертельними, однаково призводили до серйозних порушень експресії генів та інших аномалій.
Гістони не тільки забезпечують упакування ДНК, але й відіграють важливу роль у регуляції експресії генів, перебудові хроматину тощо. Кожен із них може бути субстратом для різноманітних модифікацій: метилювання, ацетилювання, деацетилювання, АДФ-рибозилювання, фосфорилювання, глікозилювання, убіквітинування, сумолювання. Оскільки ці зміни впливають на заряд і форму гістонів, то призводять до зміни структури хроматину. Окрім того існують варіанти деяких гістонів, що відіграють особливу роль у метаболізмі ДНК.
Зміст
Структура гістонів
Корові гістони, які формують нуклеосому, а саме H2A, H2B, H3, H4, мають в своїй структурі гістоновий мотив: послідовність амінокислот з трьох a-спіралей — довшої по середині, і двох коротших, з'єднаних петлями L1 та L2. Гістоновий мотив бере участь у димеризації, і присутній не лише у гістонів еукаріот, а і у гістонів деяких архей та гістонів вірусів Marseilleviridae, як і у інших транскрипційних факторів таких як TBP. Проте гістоновий мотив відсутній у гістону H1, який натомість має в своїй структурі мотив "спіраль-поворот-спіраль із крильцем" (winged helix fold): у такого домену спіраль-поворот-спіраль має по бокам бета-складчасту структуру, що формує "крильця".
Варіанти білків гістонів
Окрім п'яти «канонічних» гістонів, існують також мінорні форми, що є видозмінами перших. Таких варіантів було найбільше виявлено для гістонів H2A і H3. Гени цих білків експресуються впродовж всього клітинного циклу, і вбудовуються у хроматин не залежно від процесу реплікації. Для цього потрібні спеціальні гістонові шаперони і комплекси ремоделювання хроматину. Варіанти гістонів можуть заміщувати бліки, яких бракує у нуклеосомах, або вбудовуватись у специфічні ділянки геному. Більшість із них, як і канонічні форми, є еволюційно консервативними, що вказує на незамінну роль у життєдіяльності клітин. Проте деякі варіанти, наприклад H2A-Bdb-подібні гістони, швидко еволюціонують і виконують тканино- і навіть клітино-специфічні функції у яєчках і мозку.
Приклади деяких варіантів гістонів
| Гістон H2A.Z |
| Гістон H2A.Z знайдений у майже всіх евкаріот. Асоційований в основному із транскрипційно активними ділянками. Його функції до кінця не з'ясовані, ймовірно, що він бере участь у встановленні і підтриманні структури промотора, сприятливої для приєднання РНК-полімерази II. Також існують дані про те, що наявність цього варіанту гістона у нуклеосомах перешкоджає їх взаємодії одна з одною, таким чином сприяючи більш відкритому стану хроматину. У людини та у миші є два варіанти гістону H2A.Z: H2A.Z.1 та H2A.Z.2, які відрізняються лише на 3 амінокислотні залишки, проте кодуються двома різними генами |
| Гістон H2A.X |
| Гістон H2A.X пов'язаний із репапрацією і рекомбінацією ДНК. Нестача цього білка у мишей має наслідком генетичну нестабільність і чоловічу безплідність. Невеликі кількості нуклеосом, що містять H2AX, розкидані по всьому геному; якщо поблизу такої нуклеосоми стається двонитковий розрив ДНК, H2AX фосфорилюється по залишку Ser139, що розташований у SQ-мотиві на C-кінці. Остання подія необхідна для збирання апарату репарації у цьому місці |
| Гістон MacroH2A |
| Гістон MacroH2A є варіантом H2A, що є специфічним тільки для хребетних тварин. Місить великий «макродомен» на C-кінці. Бере участь в інактивації X-хромосоми у гомогаметної статі. |
| Гістон H2A.Bdb |
| Гістон H2A.Bdb — варіант, наявний тільки у людини, експресуюється у яєчках і головному мозку. Функції H2A.Bdb не з'ясовані. |
| Гістон H2A.Lap1 |
| Гістон H2A.Lap1 — це мишача ізоформа H2A.Bdb, експресується у тих же органах. Відома роль цього варіанту у просторовій і часовій активації генів, специфічних для тканини яєчок. |
| Гістон H3.3 |
| Гістон H3.3 — варіант гістону H3 і заміщує його в транскрипційно активних ділянках. |
| Гістон CenH3 |
| Гістон CenH3 — варіант гістону H3, наявний у ділянках центромер. CenH3 — загальна назва, що позначає білки Cse4 у дріжджів, CENPA у людей і мишей, Cid у дрозофіли тощо. Цей гістон необхідний для збирання кінетохорів, до яких кріпляться нитки веретена поділу. |
| Гістон H1oo |
| Гістон H1oo — варіант гістону H1, який присутній в ооцитах. Висококонсервативний, проте його роль не докінця з'ясована. |
Гени гістонів
Гени корових гістонів, що формують стандартну нуклеосому — H2A, H2B, H3 та H4 — разом з лінкерним гістоном H1 розміщуються в еукаріотів у вигляді кластерів у геномі. Вони експресуються залежно від стадії клітинного циклу, їх транскрипція починається з настанням S-фази, деградація їх мРНК виникає в кінці S-фази, тому ці п'ять гістонів ще називають залежними від ДНК-реплікації (англ. replication-dependent histones). В контролі деградації мРНК гістонів важливу роль грає урідинування РНК..

Матричні РНК цих гістонів — єдині мРНК евкаріотів, у яких не відбувається поліаденілування і немає поліА-хвоста. Замість цього під час процесингу мРНК гістонів формується шпилька на 3'-кінці. Зі шпилькою з'єднується білок SLBP (англ. stem-loop binding protein), який бере участь у експорті мРНК до цитоплазми, де транслюються гістони, які потім імпортуються назад до ядра. У мРНК гістонів також відсутні інтрони, а нетрансльовані послідовності відносно короткі..
Проте інші гістонові варіанти, як то MacroH2A, експресуються незалежно від циклу клітини і мають стандартну мРНК.
Модифікації білків-гістонів
«Хвости» гістонів, тобто їх N-кінцеві послідовності, що виступають назовні нуклеосоми, можуть бути місцями різноманітних посттрансляційних модифікацій (ПТМ) — приєднання певних хімічних груп, таких як метильна, ацетильна, фосфатна, глікозильна, АДФ-рибозильна, а також білків убіквітину і SUMO. Ці зміни є оборотними, вони здійснюються специфічними строго регульованими ферментами і мають складні біологічні наслідки, що залежать не тільки від хімічної групи, яка приєднується, а й від її положення і загального контексту. Для гістонів були відкриті фактичні всі можливі ПТМ білків, і відкриття нових сайтів модифікації триває, проте біологічне значення не всіх цих змін доведене.
Див. також
| ||||||||||||||||||||||||||||