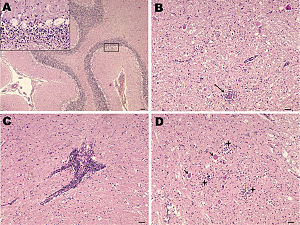
Стрибаюча хвороба
| Стрибаюча хвороба | |
|---|---|
|
Патоморфологія змін у мозку ураженої тварини
| |
| Спеціальність | інфекційні хвороби і ветеринарія |
| Причини | Louping ill virusd |
| Класифікація та зовнішні ресурси | |
| DiseasesDB | 7591 |
| MeSH | D008146 |
| | |
Стрибаюча хвороба (англ. louping or leaping ill, [ˈlaʊpɪŋɪl]; також англ. ovine encephalomyelitis, infectious encephalomyelitis of sheep, trembling-ill) — зоонозна інфекційна хвороба, яка уражає переважно овець. На неї можуть хворіти й люди. У тварин хвороба характеризується двофазною гарячкою, депресією, атаксією, порушенням м'язової координації, тремором, енцефалітом, паралічем задніх кінцівок, комою та смертю. Хвороба передається кліщами, виникнення її тісно пов'язане з поширенням основного переносника — овечого кліща Ixodes ricinus (англ. castor-bean tick — ріциновий кліщ). Серед птиць уражає помітно червоних рябчиків і тетеруків.
Внаслідок спалахів хвороби може загинути до 60 % стада жуйних тварин. У стадах більшість втрат відбувається у нещеплених молодих тварин, які більше не захищені материнськими антитілами.
Зміст
Історичні факти
Хвороба була описана у шотландських овець у XVIII столітті. Її пов'язали з передачею кліщів десь у 1830-х роках. Збудник був визнаний як вірус у 1931 році. У 1991 році хвороба людини була описана і віднесена до так званих забутих хвороб.
Етимологія
Назва «louping ill» описує стрибаючу поведінку овець, уражених вірусним енцефалітом — «лат. loup» означає «підніматися в повітря».
Етіологія
| вірус стрибаючої хвороби | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 Філограма, яка вказує на зв'язки вірусів групи кліщового енцефаліту.
| ||||||||||
| Класифікація вірусів | ||||||||||
| ||||||||||
|
Посилання
| ||||||||||
|
Вірус стрибаючої хвороби є ендеміком Британських островів, тоді як у Європі та Азії циркулює вірус кліщового енцефаліту, якій на відміну від цього вірусу не спричинює тяжких уражень у тварин. Був вперше виділений в Селкіркширі (Шотландія) в 1929 році і став першим із виділених вірусів, що передається членистоногими, в Європі.
Має 4 субтипи: британський, ірландський, іспанський і турецький. Вважалося, що це кілька споріднених вірусів (турецького енцефаліту овець, грецького енцефаліту кіз, іспанського енцефаліту овець та іспанського енцефаліту кіз). Вони описані у дрібних жуйних за межами районів, де традиційно зустрічалася стрибаюча хвороба. Хоча було запропоновано їх вважати окремими видами, деякі чи всі з цих вірусів є такими, що нині вважаються варіантами вірусу стрибаючої хвороби, адже вони мають схожих хазяїв, подібні патологічні прояви та переносників. Вірус Negishi, який був виділений в Японії в 1940-х роках, дуже схожий на вірус, який нещодавно виявили в Росії.
Як і всі представники цього роду, вірус має позитивно спрямований одноланцюговий РНК-геном завдовжки приблизно 11 kb. Секвенування повного геному вірусу показало, що він має консервативну структуру, типову для усіх Flaviviridae. Поділяється на структурні (капсид (C), премембранний (prM), оболонковий (E)) і неструктурні гени (NS1, NS2A, NS2B, NS3, NS4A, NS4B, NS5).
Після проникнення в клітину геном не розкривається і безпосередньо транслюється в один поліпептид, який протеолітично розщеплюється комбінацією протеаз, що кодуються клітиною-хазяїном і вірусом. Білок оболонки має антигенну перехресну реактивність з іншими представниками кліщових флавівірусів і є основною мішенню нейтралізуючих антитіл. Вірус, як і багато вірусів, чутливий до високої температури, дезінфікуючих засобів і кислого середовища.
Глікопротеїни оболонки обох вірусів демонструють високий ступінь ідентичності амінокислот. Дивно, але TBEV не спричинює захворювання у овець, тоді як може породити тяжкі хвороби у людей. Молекулярна філогенія на основі гена оболонки ізолятів вірусу з Британських островів припускає, що існує чотири географічно окремих лінії (генотип 1, Шотландія та Англія; генотип 2, Шотландія; генотип 3, Уельс; і генотип 4, Ірландія). Цей аналіз також припускає, що ізолят, про який повідомляється з Норвегії, походить із Великої Британії, угруповавшись із ізолятами генотипу 1 із Шотландії та Англії. Існує менше ніж 5 % нуклеотидної дивергенції в послідовності кодування оболонки між усіма досліджуваними зразками, і географічне розділення протягом багатьох років, ймовірно, сприяло наявній генетичній варіації, хоча, здається, немає ніяких змін у проявах хвороби у овець. Аналіз молекулярних послідовностей варіації гена оболонки вірусу привів до припущень, що він вперше був введений в Ірландію приблизно 800 років тому, імовірно, від попередника. Вважається, що розбіжність між вірусами виникла за останні 300 років і тісно пов'язана з переміщенням худоби на Британських островах. Молекулярно-генетичні дослідження вірусу, виділеного від іспанських кіз у 2011 році, показали, що цей ізолят на 94 % ідентичний штаму з Великої Британії, який було проаналізовано, і на 93 % ідентичний вірусу іспанського енцефаліту овець. На додаток до повної геномної послідовності, опублікованої в 1997 році, яка спочатку була виділена з інфікованого кліща, але серійно пасована в клітинній культурі перед секвенуванням, другий геном був секвенований безпосередньо зі спинного мозку вівці з ознаками неврологічного захворювання. Цей другий геном показав 95,6 % ідентичності з оригінальним геномом і 97,5 % на рівні амінокислот. Ця інформація є важливою для встановлення ступеня варіації вірусу, для розмежування членів групи флавівірусів, що переносяться кліщами, та для розуміння основних причин різних властивостей вірулентності всередині цієї таксономічної групи.
Епідеміологічні особливості
Захворювання виявляється переважно у тварин із гірських районів Великої Британії та Ірландії. Найперше уражаються барани. Клінічні випадки також спорадично задокументовані у кіз, великої рогатої худоби, коней, лам, альпак, свиней, собак, благородних оленів, козуль, зайців та деяких інших ссавців. Серопозитивні дикі лосі, благородні олені та козулі були виявлені в Норвегії. Тривалий час інформація про поширення хвороби не була достеменно вивченою, адже часто подібні прояви обумовлювала Anaplasma phagocytophilum, яка є збудником гранулоцитарного анаплазмозу, в тому числі, й у людини.
У життєвому циклі кліща I. ricinus виділяють три стадії розвитку: личинка, німфа і доросла особина. Личинкам і німфам потрібна кров перед метаморфозом на наступну стадію, а заплідненим самкам потрібна кров до розвитку яєць і відкладення яєць. У Великій Британії кліщі стають активними, коли температура піднімається вище +7 °C. Одна когорта кожної стадії життєвого циклу I. ricinus виходить із попередньої стадії наприкінці літа та восени. Ці щойно з'явилися кліщі стають активними і харчуються, якщо хазяї доступні восени, або зимують як негодовані кліщі, а замість цього харчуються навесні та на початку літа, коли температура піднімається вище порогових рівнів. Через явище діапаузи (затримка розвитку у відповідь на зміни довкілля) кліщі, які харчуються восени, не линяють до наступної осені. Ті, що живляться навесні, не зазнають діапаузи і з'являються в один і той же час, протягом осінніх місяців. Годуванню передує поведінка, яка називається пошуком, коли кліщі підіймаються рослинністю до відкритих місць і з піднятими вгору передніми кінцівками чекають випадкового контакту з господарем. Рух, тепло і вуглекислий газ, які видихає потенційний хазяїн, забезпечують атрактантів для кліщів у пошуку. Під час спекотних сухих умов, що зустрічаються влітку, кліщі у пошуку демонструють позитивний геотропізм, переміщаючись у трав'яний килимок, імовірно, щоб уникнути висихання та смерті. У цей час, якщо запаси енергії вичерпаються, кліщ загине. Дрібні ссавці, птахи та рептилії є придатними хазяїв для ювенільних стадій, але більші ссавці, зокрема вівці та олені, віддають перевагу дорослим стадіям. Весь життєвий цикл триває приблизно 3 роки, хоча може знадобитися й більше часу. Існують, як правило, сезонні моделі захворюваності навесні та наприкінці літа / осені, які збігаються з місяцями, в які живиться I. ricinus. Вірус активно реплікується в кліщі і може пережити перехід між стадіями, відомий як транстадіальна передача, але на сьогоднішній день немає доказів трансоваріальної передачі цього вірусу.
Передача через спільне годування, коли неінфіковані кліщі можуть заразитися через споживання в безпосередній близькості від інфікованого кліща, виявлена у I. ricinus, які годуються на гірських зайцях. Було багато припущень, що ссавці (крім овець), такі як гризуни, олені та зайці можуть бути резервуаром для цього вірусу. Зараженість кліщами у таких видів може бути високою. Однак досі немає переконливих доказів того, що будь-який конкретний вид є життєво важливим для підтримки циркуляції вірусу в певній місцевості.
Інфікування людей відбувається при професійному контакті з інфікованою худобою. Тваринники, працівники бойні, м'ясники та ветеринари, які контактують з вівцями або іншими потенційно інфікованими видами, піддаються найбільшому ризику. Науковці, лаборанти, які працюють з вірусом, також піддаються особливому ризику, оскільки повідомлено про низку добре задокументованих випадків лабораторної інфекції. Зараження людини від кліщів у ендемічних районах на даний момент не визначена кількісно, хоча в майбутньому таке може збільшитися через зміни соціально-економічних і кліматичних факторів, наприклад, збільшення рекреаційного використання сільської місцевості або зміни клімату, що може призвести до зміни популяції кліщів.
Патогенез
Перебіг хвороби у всіх видів схожий і відрізняється лише інтенсивністю вірусемії та частотою розвитку клінічних ознак. Після зараження інфікованим кліщем вірус спочатку розмножується в лімфоїдних тканинах, що призводить до вірусемії, яка триває 1–5 днів. Під час вірусемії може спостерігатися гарячкова реакція, але явні клінічні ознаки, як правило, відсутні, поки вірус не потрапить у ЦНС і не почне реплікацію, навіть якщо імунна відповідь елімінує вірус із екстранейрональних тканин. Ступінь нейронального пошкодження внаслідок реплікації вірусу визначає тяжкість ознак: від відсутності (субклінічні) через неврологічну дисфункцію різного ступеня до раптової смерті. Гістологічне дослідження ЦНС зазвичай показує негнійний (лімфоцитарний) поліоенцефаломієліт з ураженням у всьому мозку, але переважно в його стовбурі. Відомо про імуносупресивну дію цього мікроорганізму. Супутня патологія може бути складною та пов'язаною із вторинною бактеріальною та грибковою інфекцією, що пояснює високу летальність, яка спостерігається при виведенні на заражені кліщами пасовища.
Клінічні прояви у людей
Захворювання у людей може проявлятися по-різному. Серологічні дослідження груп ризику свідчать про те, що більшість випадків зараження перебігає безсимптомно або призводить до грипоподібного захворювання з гарячкою, головним болем і м'язовою скутістю. У деяких випадках це супроводжується подальшим періодом підвищення температури з більш серйозними неврологічними ознаками, представлені як захворювання, подібне до поліомієліту.
Причина відсутності зареєстрованих випадків захворювання людей протягом останніх кількох десятиліть неясна, хоча щорічно повідомляють про численні випадки енцефаліту невідомого походження), хоча деякі можуть являти собою випадки стрибаючої хвороби. Можливо, недостатня поінформованість клініцистів або відсутність специфічного тестування могли спричинити відсутність зареєстрованих випадків.
Є свідчення про можливість поодиноких випадків клінічного перебігу за типом геморагічної гарячки.
Хвороба у тварин
Інкубаційний період коливається від 6 до 18 днів у овець. У парентерально прищеплених рябчиків клінічні ознаки розвинулися на 2-8 добу. Перебіг інфекції у всіх видів схожий і відрізняється лише інтенсивністю вірусемії та частотою розвитку клінічних ознак.
У овець хвороба характеризується початковою гарячковою стадією, під час якої у тварин можуть виникати неспецифічні ознаки, такі, як депресія та анорексія, а потім у деяких тварин незначні (наприклад, транзиторна атаксія) чи, навіть, тяжкі неврологічні прояви. Гарячка не постійно присутня протягом другої, неврологічної стадії. У отарах овець летальність коливається від 60 % у новопривезених поголів'ях, до 5–10 % у овець, які акліматизувалися на пасовищі.
Велика рогата худоба також іноді заражається і має неврологічні прояви. Захворювання коней включає атаксію, м'язовий тремор і підвищену збудливість. У всіх випадках уражені коні одужали з високим титром антитіл проти вірусу.
Джерела
- C. L. Jeffries, K. L. Mansfield, L. P. Phipps, P. R. Wakeley, R. Mearns, A. Schock, S. Bell, A. C. Breed, A. R. Fooks, N. Johnson Louping ill virus: an endemic tick-borne disease of Great Britain. J Gen Virol. 2014 May 1; 95(Pt 5): 1005—1014. doi: 10.1099/vir.0.062356-0 PMCID: PMC4811648 PMID 24552787 [1] (англ.)
- Louping ill. Center for Food Security and Public Health, College of Veterinary Medicine, Iowa State University, 2005-08-05 [2] [Архівовано 30 листопада 2021 у Wayback Machine.] (англ.)
Посилання
- Meaning of LOUPING ILL in English [Архівовано 30 грудня 2021 у Wayback Machine.] (англ.)
- Intestinal Diseases in Sheep and Goats [Архівовано 29 жовтня 2021 у Wayback Machine.]
- LOUPING ILL — UK: VACCINATION (англ.)
|