Кон'югат антитіла з лікарським засобом
Кон'югат антитіла з лікарським засобом — це клас біофармацевтичних препаратів, розроблених як цільова терапія для лікування злоякісних пухлин. На відміну від хіміотерапії, кон'югати антитіла з лікарським засобом направлені для цільового знищення пухлинних клітин, зберігаючи здорові клітини. Станом на 2019 рік близько 56 фармацевтичних компаній розробляли кон'югати антитіла з лікарським засобом.
Кон'югат антитіла з лікарським засобом є складною молекулою, що складаються з антитіла, пов'язаного з біологічно активним цитотоксичним (протипухлинним) корисним доповненням або препаратом. Кон'югати антитіла з лікарським засобом є прикладами біокон'югатів та імунокон'югатів.
Кон'югати антитіла з лікарським засобом поєднують націленість моноклональних антитіл із здатністю цитотоксичних препаратів вбивати ракові клітини. Вони можуть також розроблятися й для розрізнення здорової та хворої тканини.
Зміст
Механізм дії
Протипухлинний препарат з'єднується з антитілом, яке специфічно спрямоване на певний пухлинний антиген (наприклад, білок, який можна виявити лише в пухлинних клітинах або на їх поверхні). Антитіла прикріплюються до антигенів на поверхні ракових клітин. Біохімічна реакція між антитілом і білком мішені (антигеном) запускає сигнал в пухлинній клітині, яка пізніше поглинає або впускає всередину антитіло разом із пов'язаним цитотоксином. Після того, як кон'югат засвоюється, цитотоксин вбиває пухлинну клітину. Таке цільове застосування обмежує кількість побічних ефектів, і дає ширше терапевтичне вікно, ніж інші хіміотерапевтичні засоби.
Технології створення кон'югатів антитіла з лікарським засобом були представлені в багатьох публікаціях, зокрема й у низці наукових журналів.
Історія створення
Ліки, які були б спрямовані на пухлинні клітини та не діяли б на інші клітини, були задумані ще в 1900 році німецьким ученим, лауреатом Нобелівської премії Паулем Ерліхом.
У 2001 році препарат компаній «Pfizer» і «Wyeth» гемтузумаб озогаміцин (торгова назва: «Майлотарг») отримав схвалення FDA на основі дослідження із сурогатною кінцевою точкою за прискореною процедурою схвалення. У червні 2010 року, після того, як були накопичені докази, на основі яких показана відсутність користі та значної токсичності препарату, FDA змусило компанію відкликати препарат з ринку. У 2017 році гемтузумаб озогаміцин був знову допущений на ринок США.
Брентуксимаб ведотин (торгова назва: «Адцетрис», маркетинг препарату проводиться компаніями «Seattle Genetics» і «Takeda Pharmaceutical») отримав схвалення FDA 19 серпня 2011 року для лікування рецидиву лімфогранульоматозу та рецидиву неходжкінської лімфоми та отримав умовну реєстрацію від Європейського агентства з лікарських засобів у жовтні 2012 року.
Трастузумаб емтанзин (адо-трастузумаб емтанзин або T-DM1, торгова назва «Кадцила», маркетинг проводиться «Genentech» і «Roche») схвалений у лютому 2013 року для лікування хворих з HER2-позитивним метастатичним раком молочної залози, які отримували попереднє лікування трастузумабом і хіміотерапію таксанами.
Європейська комісія 30 червня 2017 року схвалила інотузумаб озогаміцин як монотерапію для лікування дорослих із рецидивуючим або рефрактерним CD22-позитивним В-клітинним гострим лімфобластним лейкозом під торговою назвою «Безпонса®» (компаній «Pfizer»/«Wyeth»), після чого 17 серпня 2017 року його схвалило FDA.
Перший імунологічний кон'югат антитіла з лікарським засобом ABBV-3373 продемонстрував зниження активності хвороби у клінічному дослідженні ІІа фази хворих з ревматоїдним артритом, також з позитивними результатами пройшла перша фаза дослідження з іншим подібним кон'югатом антитіла з лікарським засобом ABBV-154, в якому проводилась оцінка побічних явищ та зміна активності захворювання у учасників, які отримували підшкірну ін'єкцію ABBV-154, дослідження ще триває.
У липні 2018 року компанії «Daiichi Sankyo» та «Glycotope GmbH» уклали угоду щодо дослідження комбінації пухлинно-асоційованого антитіла TA-MUC1 гатіпотузумабу компанії «Glycotope» та технології компанії «Daiichi Sankyo» для розробки кон'югату антитіл з лікарським засобом.
У 2019 році «AstraZeneca» погодилася виплатити до 6,9 мільярдів доларів США за спільну розробку препарату DS-8201 з японською компанією «Daiichi Sankyo». Він призначений для заміни герцептину для лікування раку молочної залози. DS8201 має у своєму складі 8 корисних включень у порівнянні з 4 у більшості кон'югатів антитіла з лікарськими засобами.
Торгові марки
Загалом 11 кон'югатів антитіла з лікарським засобом отримали схвалення для клінічного застосування — усі для лікування злоякісних пухлин.
| Препарат | Виробник | Хвороба | Торгова назва |
|---|---|---|---|
| Гемтузумаб озогаміцин | Pfizer/Wyeth | Гострий мієлобластний лейкоз | Майлотарг |
| Брентуксимаб ведотин | Seattle Genetics, «Millennium»/«Takeda Pharmaceutical» | Лімфогранульоматоз та неходжкінська лімфома | Адцетрис |
| Трастузумаб емтанзин | «Genentech», «Roche» | HER2-позитивний метастатичний рак молочної залози після лікування трастузумабом і майтанзиноїдом | Кадцила |
| Інотузумаб озогаміцин | «Pfizer»/«Wyeth» | Рецидивуючий або рефрактерний CD22-позитивний В-клітинний гострий лімфобластний лейкоз | Безпонса |
| Полатузумаб ведотин | «Genentech», «Roche» | Рецидивуюча або рефрактерна дифузна великоклітинна В-клітинна лімфома | Поліві |
| Енфортумаб ведотин | «Astellas»/«Seattle Genetics» | Дорослі хворі з локально поширеним або метастатичним епітеліальним раком сечових шляхів, які отримували інгібітори PD-1 або PD-L1 і Pt-вмісну терапію | Падсев |
| Трастузумаб дерукстекан | «AstraZeneca»/«Daiichi Sankyo» | Дорослі хворі з неоперабельним або метастатичним HER2-позитивним раком молочної залози, які отримували дві або більше попередніх схем на основі анти-HER2 | Енгерту |
| Сацитузумаб говітекан | «Immunomedics» | Дорослі хворі метастатичним потрійно негативним раком молочної залози, які отримували принаймні 2 попередні курси терапії, або хворі з рецидивом або рефрактерним раком з метастазуванням | Тродельві |
| Белантамаб мафодотин | «GlaxoSmithKline» | Хворі з множинною мієломою із прогресуванням хвороби, незважаючи на попереднє лікування імуномодулюючим засобом, інгібітором протеасоми та антитілами до CD38 | Бленреп |
| Моксетумомаб пасудотокс | «AstraZeneca» | Рецидивний або рефрактерний волохатоклітинний лейкоз | Люмокситі |
| Лонкастуксимаб тезирин | «ADC Therapeutics» | Рецидивуюча або рефрактерна великоклітинна В-клітинна лімфома (включаючи дифузну великоклітинну В-клітинну лімфому, не зазначену інакше, як низькодиференційовану лімфому, так і високодиференційовану В-клітинну лімфому) після 2 або більше курсів системної терапії | Зінлонта |
| Тизотумаб ведотин-tftv | «Seagen Inc» | Дорослі хворі з рецидивуючим або метастатичним раком шийки матки з прогресуванням хвороби під час або після хіміотерапії | Тівідак |
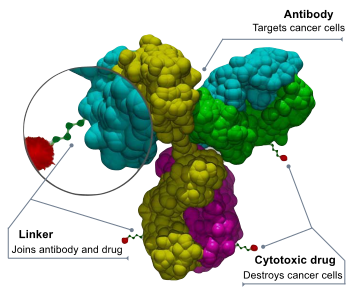
Склад кон'югата антитіла з лікарським засобом
Кон'югат антитіла з лікарським засобом складається з 3 компонентів: антитіла, яке націлено на мішень препарату, і може також спричинювати лікувальну дію. Корисне включення — спричинює бажану лікувальну дію. Лінкер — це низькомолекулярна сполука, яка приєднує корисне включення до антитіла, та має бути стабільним у кровоносному руслі, лише вивільняючи корисне включення на мішень препарату. Для приєднання до антитіла було розроблено та розглянуто кілька підходів до кон'югації. Для кон'югату антитіла з лікарським засобом вираховується також співвідношення DAR, яке означає рівень співвідношення ліків і антитіл, та вказує на рівень наповненості корисним включенням кон'югату антитіла з лікарським засобом.
Корисні включення
Багато корисних включень для онкологічних кон'югатів антитіла з лікарським засобом є природними засобами, що мають здатність встановлювати ковалентні зв'язки задля нейтралізації їх мішені. Корисні включення включають інгібітори мікротубуліну монометил ауристатин E, монометил ауристатин F і мертанзин, ДНК-зв'язуючу речовину каліхеаміцин та інгібітори топоізомерази 1 SN-38 і ексатекан, що призвело до ренесансу використання природних засобів у хіміотерапії. Модулятори глюкокортикоїдних рецепторів є найбільш активним класом корисних включень до кон'югатів антитіла з лікарським засобом. Були розроблені підходи до включення до складу кон'югатів давно синтезованих модуляторів глюкокортикоїдних рецепторів, зокрема дексаметазону та будесоніду. Також були розроблені модифіковані молекули модуляторів глюкокортикоїдних рецепторів, які дозволяють оптимізувати процес приєднання лінкера до корисного включення. Досліджувалась також альтернатива низькомолекулярних корисних включень, зокрема малі інтерферуючі РНК.
Лінкери
Стабільний зв'язок між антитілом і цитотоксичним (протираковим) агентом є вирішальним аспектом ефективності кон'югату антитіла з лікарським засобом. Стабільний лінкер кон'югату гарантує, що буде втрачено менше цитотоксичного корисного включення, перш ніж воно досягне пухлинної клітини, покращиться безпечність препарату, та зменшиться необхідна доза препарату.
Лінкери є представниками кількох класів хімічних речовин, включаючи дисульфіди, гідразони або пептиди (розщеплювані сполуки) або тіоетери (нерозщеплювані сполуки). Під час доклінічних і клінічних досліджень було доведено, що лінкери, як ті, що розщеплюються, так і ті, що не розщеплюються, є безпечними. Брентуксимаб ведотин включає до свого складу чутливий до ферментів лінкер, що розщеплюється, який доставляє інгібітор мікротубуліну монометил ауристатин Е, що є синтетичним протипухлинним засобом, до специфічних для людини CD30-позитивних клітин злоякісних пухлин. Mонометил ауристатин E пригнічує поділ клітин, блокуючи полімеризацію тубуліну. У зв'язку з високою токсичністю монометил ауристатин E не можна застосовувати як самостійний хіміотерапевтичний препарат. Однак монометил ауристатин E, пов'язаний з моноклональним антитілом проти CD30 (cAC10, білком клітинної мембрани фактора некрозу пухлини або рецептором TNF), був стабільним у позаклітинній рідині. Він розщеплюється катепсином і безпечний для застосування в лікуванні. Трастузумаб емтанзин є комбінацію інгібітора утворення мікротрубочок мертанзину та антитіла трастузумабу, яка використовує стабільний нерозщеплюваний лінкер.
Наявність кращих і стабільніших лінкерів змінила функцію хімічного зв'язку. Тип лінкера, розщеплюваний або нерозщеплюваний, надає цитотоксичному препарату специфічні властивості. Зокрема, нерозщеплюваний лінкер утримує препарат у клітині. Унаслідок цього все антитіло, лінкер і цитотоксичний (протираковий) агент потрапляють в цільову ракову клітину, де антитіло розкладається до амінокислоти. Отриманий комплекс — амінокислота, лінкер і цитотоксичний агент — вважається активним препаратом. Навпаки, лінкери, що розщеплюються, від'єднуються ферментами в раковій клітині. Цитотоксичне корисне включення може вийти з цільової клітини і в процесі, який називається «вбивство сторонніх», атакувати сусідні клітини.
Інший тип розщеплюваного лінкера, який знаходиться в розробці, додає додаткову молекулу між цитотоксином і сайтом розщеплення. Це дозволяє дослідникам створювати кон'югати антитіла з лікарським засобом з більшою гнучкістю, не змінюючи кінетику розщеплення. Дослідники розробляють новий метод розщеплення пептидів, заснований на методі секвенування амінокислот у пептиді, названий розщепленням за Едманом. Також розробляються сайт-специфічна кон'югація, та нові методи кон'югації для подальшого покращення стабільності та терапевтичної активності кон'югату, імунокон'югати, що випромінюють α-частинки, наночастинки, кон'юговані з антитілами, та кон'югати антитіло-олігонуклеотиди.
Новітні форми кон'югата антитіла з лікарським засобом
Оскільки з'явились нові форми конюгату антитіла з лікарським засобом, можливе точніше визначення точніше визначення цієї форми препарату, яке може звучати як «кон'югат чогось із лікарським засобом». Альтернативами стандартних антитіл включають декілька менших фрагментів антитіл, зокрема діатіла, Fab, scFV, та біциклічні пептиди.
Дослідження
Неприродні амінокислоти
Перше покоління кон'югатів антитіла з лікарським засобом використовують технології зв'язування, за допомогою яких неселективно зв'язують ліки із залишками цистеїну або лізину в антитілах, внаслідок чого утворюється гетерогенна суміш. Такий підхід призводить до неоптимальної безпеки застосування препарату і його ефективності, та ускладнює оптимізацію біологічних, фізичних та фармакологічних властивостей. Сайт-специфічне включення неприродних амінокислот створює сайт для контрольованого та стабільного приєднання. Це дозволяє створювати однорідні кон'югати з антитілами, вивірено пов'язаними з препаратом, і контрольованим співвідношенням антитіла до препарату, що дозволяє вибрати найкращий у своєму класі кон'югат антитіла з лікарським засобом. Відкритий безклітинний синтез на основі Escherichia coli дозволяє синтезувати білки, що містять специфічно включені неприродні амінокислоти, та оптимізований для передбачуваного високопродуктивного синтезу та згортання білка. Відсутність клітинної стінки дозволяє додавати до системи неприродні фактори, щоб керувати транскрипцією, трансляцією та згортанням білка для забезпечення точної модуляції експресії білка.
Інші галузі медицини
Більшість кон'югатів антитіла з лікарським засобом, які розробляються або перебувають у клінічних випробуваннях, призначені для застосування при онкологічних та гематологічних захворюваннях. Це в першу чергу обумовлено наявністю моноклональних антитіл, мішенню яких є різні типи раку. Однак деякі розробники прагнуть розширити застосування кон'югатів антитіла з лікарським засобом для інших груп захворювань.